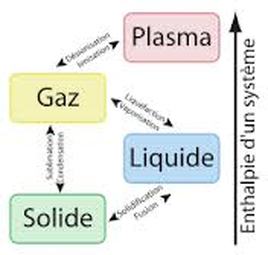
Module 1- Les Gaz
Au quotidien , les gaz jouent un rôle primordial dans nos vies. L'étude des gaz nous permettra de mieux comprendre le monde qui nous entoure.
Chapitre 1- Propriétés physiques des gaz
La vapeur (DÉF)
Le terme "vapeur" est utilisé dans des cas particuliers. Le mot "vapeur" signifie une substance qui aux conditions ambiantes est habituellement solide ou liquide mais elle peut aussi être retrouvée sous la forme gazeuse. Exemples: Vapeur d'eau, vapeur de mercure, vapeur d'iode.
Attention! On ne parle pas de vapeur d'azote car N2 est gazeux aux conditions ambiantes.
Attention! On ne parle pas de vapeur d'azote car N2 est gazeux aux conditions ambiantes.
THÉORIE CINÉTIQUE des gaz
Énergie cinétique (déf)
ÉNERGIE ASSOCIÉE AU MOUVEMENT DES CORPS en physique ou DES PARTICULES EN CHIMIE.
FORMULE: EK = 1/2MV2
m représente la masse (g) et v la vitesse (m/s)
Il faut savoir et retenir!
L'énergie cinétique dépend de la masse et de la vitesse des particules qui composent la substance. Dans les mêmes conditions (P,V,n,T constants), l'énergie cinétique moyenne est constante. Attention! Les particules ne se déplacent pas à vitesse constante tout le temps, lors de collisions Ek diminue temporairement. ce qui fait en sorte que certaines particules ralentissent pendant que d'autres accélèrent.
COURBE DE BOLTZMANN
Ludwig Boltzmann a réussi à établir la relation qui illustre la répartition du nombre de particules en fonction de leur vitesse à un moment donné dans un échantillon de gaz.
Questionnement:
Si l'on te remet 2 échantillons de gaz différents (H2 et N2) dans les mêmes conditions (P,V,n,T constants) ils auront la même énergie cinétique moyenne. Explique comment cela est-il possible? Explique.
Qu'arrivera-t-il à l'énergie cinétique moyenne du gaz si... a) j'augmente la masse de l'échantillon b) j'augmente la température de l'échantillon Discute.
FORMULE: EK = 1/2MV2
m représente la masse (g) et v la vitesse (m/s)
Il faut savoir et retenir!
L'énergie cinétique dépend de la masse et de la vitesse des particules qui composent la substance. Dans les mêmes conditions (P,V,n,T constants), l'énergie cinétique moyenne est constante. Attention! Les particules ne se déplacent pas à vitesse constante tout le temps, lors de collisions Ek diminue temporairement. ce qui fait en sorte que certaines particules ralentissent pendant que d'autres accélèrent.
COURBE DE BOLTZMANN
Ludwig Boltzmann a réussi à établir la relation qui illustre la répartition du nombre de particules en fonction de leur vitesse à un moment donné dans un échantillon de gaz.
Questionnement:
Si l'on te remet 2 échantillons de gaz différents (H2 et N2) dans les mêmes conditions (P,V,n,T constants) ils auront la même énergie cinétique moyenne. Explique comment cela est-il possible? Explique.
Qu'arrivera-t-il à l'énergie cinétique moyenne du gaz si... a) j'augmente la masse de l'échantillon b) j'augmente la température de l'échantillon Discute.
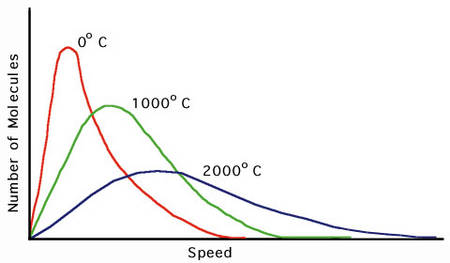
L'effet d'une augmentation de la température sur la courbe de Boltzmann
Explication: Une augmentation de la température augmente le niveau d'agitation des particules augmentant ainsi la vitesse moyenne des particules du système. La courbe est déplacée vers la droite, illustrant ainsi l'augmentation de la vitesse moyenne des particules. Il est à noter que le dessin de la courbe à T plus élevée commence sous la première et se termine par dessus la première illustrant qu'il y a moins de particules ayant une petite vitesse et plus de particules ayant une plus grande vitesse qu'à un température plus petite. Essaie de dessiner et d'expliquer l'effet d'une diminution de la température.
Explication: Une augmentation de la température augmente le niveau d'agitation des particules augmentant ainsi la vitesse moyenne des particules du système. La courbe est déplacée vers la droite, illustrant ainsi l'augmentation de la vitesse moyenne des particules. Il est à noter que le dessin de la courbe à T plus élevée commence sous la première et se termine par dessus la première illustrant qu'il y a moins de particules ayant une petite vitesse et plus de particules ayant une plus grande vitesse qu'à un température plus petite. Essaie de dessiner et d'expliquer l'effet d'une diminution de la température.
Les 4 points de la théorie cinétique des gaz
1- Les gaz sont faits de particules extrêmement petites espacées par du vide.
2- Les particules de gaz bougent constamment en ligne droite dans toutes les directions.
3- Si une particule de gaz rencontre un obstacle, elle rebondit sans perdre d'énergie.
4- L'énergie cinétique moyenne dépend de la température.
Wikipédia: Théorie cinétique des gaz
La température d'un gaz parfait monoatomique est une mesure de l'énergie cinétique moyenne des particules qui le constituent. Cette animation montre le mouvement des atomes d'hélium à 5 000 K, sous une pression de 1 950 atm ; la taille des atomes d'hélium et leur distances sont à l'échelle et la vitesse de déplacement des particules a été ralentie deux milliards de fois.
OBSERVATION: Pour définir un gaz, on utilise 4 variables: P (pression) T (température) V (volume) et n (nombre de particules)
Réflexions...
Qu'arrive-t-il à un système gazeux (si V et n constants) et que l'on augmente la température ?
L'effet d'une variation de température sur le comportement des molécules de gaz: Lorsque l'on réchauffe un gaz, le niveau d'agitation des molécules augmente, les molécules se déplacent de plus en plus rapidement, leur vitesse augmente. Comme le volume est constant et le nombre de particules aussi, une augmentation de température provoque aussi une augmentation du nombre de collisions sur les parois ce qui explique une augmentation de pression du système.
Qu'arrive-t-il à l'énergie cinétique moyenne du gaz? L'énergie cinétique du système augmente (Ek= 1/2 mv2) à cause de la vitesse moyenne des particules qui augmente.
Réflexions...
Qu'arrive-t-il à un système gazeux (si V et n constants) et que l'on augmente la température ?
L'effet d'une variation de température sur le comportement des molécules de gaz: Lorsque l'on réchauffe un gaz, le niveau d'agitation des molécules augmente, les molécules se déplacent de plus en plus rapidement, leur vitesse augmente. Comme le volume est constant et le nombre de particules aussi, une augmentation de température provoque aussi une augmentation du nombre de collisions sur les parois ce qui explique une augmentation de pression du système.
Qu'arrive-t-il à l'énergie cinétique moyenne du gaz? L'énergie cinétique du système augmente (Ek= 1/2 mv2) à cause de la vitesse moyenne des particules qui augmente.
Comparons maintenant 2 systèmes gazeux. qui sont définis par 4 variables identiques: P,T, V, et n sont constants pour les deux systèmes.
Les deux systèmes ont-ils la même masse? Non, ils contiennent le même nombre de molécules (n) mais le gaz ayant la plus grande masse molaire moléculaire est plus lourd que l'autre ayant la plus petite masse molaire moléculaire. Ex: N2 plus léger que CO2.
Les deux systèmes ont-ils la même énergie cinétique moyenne? Oui, ils sont à la même température dons ils ont la même énergie cinétique moyenne. Ceci s'explique par le fait que le gaz le plus lourd (masse plus grande) bouge moins rapidement (vitesse plus petite) que le gaz léger (masse plus petite) qui bouge plus rapidement (vitesse plus grande) d'où Ek1 = Ek2 .
Les deux systèmes ont la même pression, comment l'expliquer? Les particules du gaz le plus lourd se déplacent moins rapidement, elles cognent les parois du contenant moins souvent mais plus fortement par opposition au gaz plus léger dont les particules moins lourdes se déplacent plus rapidement, elles cognent les parois plus souvent mais moins fortement ainsi la pression ressentie dans chaque système est la même.
Les deux systèmes ont-ils la même masse? Non, ils contiennent le même nombre de molécules (n) mais le gaz ayant la plus grande masse molaire moléculaire est plus lourd que l'autre ayant la plus petite masse molaire moléculaire. Ex: N2 plus léger que CO2.
Les deux systèmes ont-ils la même énergie cinétique moyenne? Oui, ils sont à la même température dons ils ont la même énergie cinétique moyenne. Ceci s'explique par le fait que le gaz le plus lourd (masse plus grande) bouge moins rapidement (vitesse plus petite) que le gaz léger (masse plus petite) qui bouge plus rapidement (vitesse plus grande) d'où Ek1 = Ek2 .
Les deux systèmes ont la même pression, comment l'expliquer? Les particules du gaz le plus lourd se déplacent moins rapidement, elles cognent les parois du contenant moins souvent mais plus fortement par opposition au gaz plus léger dont les particules moins lourdes se déplacent plus rapidement, elles cognent les parois plus souvent mais moins fortement ainsi la pression ressentie dans chaque système est la même.
La diffusion et l'effusion
Naturellement, un gaz se déplace d'un milieu à plus forte concentration vers un milieu à plus faible concentration à cause de son niveau constant d'agitation, les collisions entre les molécules de gaz font en sorte que les particules de gaz sont redirigées suite à une collision et elles finissent par occuper tout l'espace disponible. Ex. un parfum, une odeur bonne ou mauvaise finit toujours par se propager... tous finissent par sentir l'odeur mais après un certain temps l'odeur s'atténue car la concentration des particules diminue dans l'espace.
Diffusion (déf) phénomène associé à la dispersion aléatoire des particules de gaz dans l'espace. Le processus de diffusion est relativement lent même si les particules se déplacent rapidement dû aux nombreuses collisions qui changent la trajectoire des particules constamment. Revoir démonstartion NH3 et HCl dans un tube de verre.
Effusion (déf) processus par lequel un gaz passe à travers une paroi par un petit trou pour se propager dans l'espace.
Considérant 2 gaz différents comme le NH3 et le HCl. Lequel des deux gaz diffuse le plus rapidement? NH3 car sa masse molaire moléculaire est plus petite que le HCl qui est plus lourd et qui se déplace plus lentement.
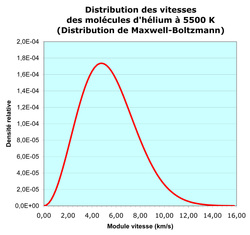
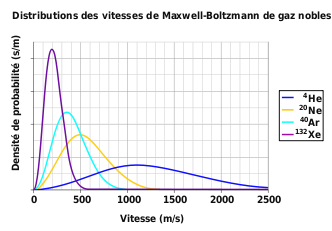
COURBE DE BOLTZMANN POUR LES GAZ INERTES (Attention! cette courbe a la vitesse en abcisse et non l'énergie cinétique)
Explications: Les gaz qui ont une masse molaire moléculaire moins grande diffusent plus rapidement que les gaz plus lourds. Les courbes du schéma ci-contre illustre ce phénomène pour les gaz inertes. L'hélium est représenté par la courbe bleue plus basse dont la vitesse moyenne est supérieure à la vitesse moyenne de la courbe violette du xénon beaucoup plus à gauche avec un pic plus prononcé déplacé vers les plus petites vitesses. L'hélium (4,00g/mol) est un gaz beaucoup plus léger que le xénon (131,29g/mol)
Diffusion (déf) phénomène associé à la dispersion aléatoire des particules de gaz dans l'espace. Le processus de diffusion est relativement lent même si les particules se déplacent rapidement dû aux nombreuses collisions qui changent la trajectoire des particules constamment. Revoir démonstartion NH3 et HCl dans un tube de verre.
Effusion (déf) processus par lequel un gaz passe à travers une paroi par un petit trou pour se propager dans l'espace.
Considérant 2 gaz différents comme le NH3 et le HCl. Lequel des deux gaz diffuse le plus rapidement? NH3 car sa masse molaire moléculaire est plus petite que le HCl qui est plus lourd et qui se déplace plus lentement.
COURBE DE BOLTZMANN POUR LES GAZ INERTES (Attention! cette courbe a la vitesse en abcisse et non l'énergie cinétique)
Explications: Les gaz qui ont une masse molaire moléculaire moins grande diffusent plus rapidement que les gaz plus lourds. Les courbes du schéma ci-contre illustre ce phénomène pour les gaz inertes. L'hélium est représenté par la courbe bleue plus basse dont la vitesse moyenne est supérieure à la vitesse moyenne de la courbe violette du xénon beaucoup plus à gauche avec un pic plus prononcé déplacé vers les plus petites vitesses. L'hélium (4,00g/mol) est un gaz beaucoup plus léger que le xénon (131,29g/mol)
La pression
(déf) la pression correspond à la force exercée perpendiculairement par unité de surface.
P pression (Pa) = F force (N) ou mg m: masse (kg) et g: 9,8N/kg
A aire de la surface (m2)
Pression normale (règle d'équivalence) : 101,3 kPa ou 1 atmosphère ou 760 mm de Hg
La pression d'un gaz dépend de la force et du nombre de collisions des particules de gaz avec les parois dans lequel le gaz se retrouve.
Exemple: Deux gaz dans les mêmes conditions de T (n et V constants) auront la même pression p.c.q... Un gaz plus léger (MMM plus petite) frappera les parois avec une force plus petite (plus petite masse) mais plus souvent (vitesse plus rapide) que le gaz plus lourd (MMM plus élevée) qui lui frappera plus fort mais moins souvent car plus lourd alors moins vite.
P pression (Pa) = F force (N) ou mg m: masse (kg) et g: 9,8N/kg
A aire de la surface (m2)
Pression normale (règle d'équivalence) : 101,3 kPa ou 1 atmosphère ou 760 mm de Hg
La pression d'un gaz dépend de la force et du nombre de collisions des particules de gaz avec les parois dans lequel le gaz se retrouve.
Exemple: Deux gaz dans les mêmes conditions de T (n et V constants) auront la même pression p.c.q... Un gaz plus léger (MMM plus petite) frappera les parois avec une force plus petite (plus petite masse) mais plus souvent (vitesse plus rapide) que le gaz plus lourd (MMM plus élevée) qui lui frappera plus fort mais moins souvent car plus lourd alors moins vite.
La mesure de la pression d'un gaz (le manomètre)
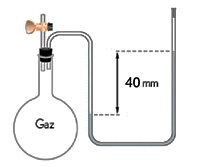
Manomètre à bout fermé (Pression absolue)
la lecture se fait directement sur l'échelle, la pression
du gaz est égale à la différence de hauteur du liquide
dans le tube en U.
Pgaz = h
Dans l'exemple, Pgaz = 40 mm Hg
la lecture se fait directement sur l'échelle, la pression
du gaz est égale à la différence de hauteur du liquide
dans le tube en U.
Pgaz = h
Dans l'exemple, Pgaz = 40 mm Hg
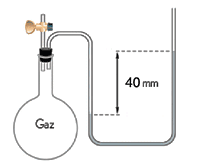
Manomètre à bout ouvert (Pression relative)
la lecture doit tenir compte de la poussée de l'atmosphère à l'une des extrémités du tube.
2 situations possibles:
1- Pgaz est plus gande que Patm
Pgaz = Patm + h
2- Pgaz est plus petite que Patm
Pgaz = Patm - h
Dans l'exemple, Pgaz est plus gande que Patm
Pgaz = Patm + h
Si Patm = 760 mm Hg
Pgaz = 760 + 40 = 800 mm Hg
la lecture doit tenir compte de la poussée de l'atmosphère à l'une des extrémités du tube.
2 situations possibles:
1- Pgaz est plus gande que Patm
Pgaz = Patm + h
2- Pgaz est plus petite que Patm
Pgaz = Patm - h
Dans l'exemple, Pgaz est plus gande que Patm
Pgaz = Patm + h
Si Patm = 760 mm Hg
Pgaz = 760 + 40 = 800 mm Hg
| la_manomètre_et_la_pression_des_gaz_sur_weebly.pptx | |
| File Size: | 167 kb |
| File Type: | pptx |
La loi de Graham
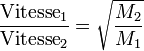
Au laboratoire, nous avons pu observer dans un tube de verre que 2 gaz différents ne diffusent pas à la même vitesse c.à.d plus le gaz est léger plus il se propage rapidement et l'inverse plus un gaz est lourd plus il se déplace lentement. L'ammoniac NH3 (17,04g/mol) est plus rapide que le HCl (36,46g/mol) qui est le plus lourd. La distance parcourue dans le tube par l'ammoniac est grande que celle parcourue par le HCl.
Thomas Graham en 1833 stipule que 2 gaz différents dans les mêmes conditions de température et de pression ont la même énergie cinétique moyenne. Voici le loi qui en découle...
On s'aperçoit que le rapport des vitesses de propagation est inversement proportionnel à la racine carré des masses molaires.
Thomas Graham en 1833 stipule que 2 gaz différents dans les mêmes conditions de température et de pression ont la même énergie cinétique moyenne. Voici le loi qui en découle...
On s'aperçoit que le rapport des vitesses de propagation est inversement proportionnel à la racine carré des masses molaires.
Ci-dessous vous verrez 3 documents: Loi de Graham théorie et exercices 1- Adobe reader- texte seulement 2 et 3- Pencast texte et paroles à écouter.
| spa7_p8_10loidegraham.pdf | |
| File Size: | 8860 kb |
| File Type: | |
|
|
|
CHAPITRE 3-
Stoechiométrie des gaz
Règle d'équivalence:
1 mole de ... = Masse molaire moléculaire (g) = 22,4L (à 0 degré celsius) ou 24,5L(à 25 degrés celsius)
Le volume molaire (théorie)
Chapitre 2- Les lois simples des gaz
Ci-dessous vous verrez 4 «pencast» sur les lois simples des gaz¨:
1- Relation P-V Loi de Boyle-Mariotte (p.2-3)
2- Relation P-T Loi de Gay-Lussac (p.4)
3- Relation V-T Loi de Charles (p.5)
4- Relation V-n Loi d'Avogadro (p.6-7)
1- Relation P-V Loi de Boyle-Mariotte (p.2-3)
2- Relation P-T Loi de Gay-Lussac (p.4)
3- Relation V-T Loi de Charles (p.5)
4- Relation V-n Loi d'Avogadro (p.6-7)
|
Relation P-V (notebook 1 p.2-3)
|
|
La loi générale des gaz |
|